Commençons par regarder une archive vidéo de l'INA qui date de 1979.
Extrait du livre de Jean Luc Perrier
Energie solaire état actuel des applications (années 1980)
_______________________________________________________________________________
12.2 L’HYDROGÈNE (Le pétrole propre de demain) (1)
L’hydrogène se présente sous la forme gazeuse à température ambiante, ou liquide en dessous de -253°C (LH2) ;
Sa valeur énergétique à pression constante : 34 000 Kcal contre 10 000 Kcal pour un produit pétrolier (essence, mazout) lui confère par exemple en aéronautique un gain de poids considérable mais un volume plus grand.
L’hydrogène n’est pas toxique, c’est l’un des corps simples le plus répandu dans la nature.
La très grande légèreté de l’hydrogène (15 fois moins lourd que l’air : densité 0,0695 par rapport à l’air) provoque une évacuation rapide des éventuelles fuites, donc moins de risque ; nous ferons une analyse de la sécurité en détail plus loin.
L’hydrogène a une conductivité thermique sept fois plus grande que l’air, c’est pourquoi on l’utilise pour le refroidissement des gros alternateurs ; PH2 est diamagnétique (répulsion par un aimant), d’une viscosité moitié moins grande que l’air et s’enflamme spontanément à partir de 585 °C
(540° C pour le méthane et seulement 228 à 471°C pour l’essence).
Contrairement à beaucoup de gaz, l’hydrogène s’échauffe si sa détente est très rapide.
l’H2 est vendu dans le commerce (Sté l’Air-Liquide, la Carboxyde Française), en bouteilles sous pression à 196 bars à l’état gazeux en trois catégories : H2 type R avec un taux > à 99,95 % ; H2 type U avec un taux > à 99,995 % ; H2 type N55 avec un taux > à 99,9995 % et l’hydrogène industriel.
Les deux premières catégories sont livrables aussi par cadres de 270 m3 ou par semi-remorques de 2 000 m3 à 196 bars. L’hydrogène liquide (LH2) est disponible en récipients de 5, 10 à 100 litres à garde d’azote sans pression, ou en réservoirs de 800 litres à 2,9 ou 10 bars ou par semi-remorques de 10 000 litres à 0,85 bar.
(1) Par « reforming » catalytique d’un hydrocarbure; solution actuelle qui donne 20 millions de tonnes d’hydrogène par an dans le monde, mais elle est coûteuse et hors de propos pour l’avenir car il faut du pétrole au départ...
(2) Par biosynthèse : Les rendements sont faibles mais des études sont en cours.
(3) Par électrolyse de l'eau avec des stations électro-solaires.
a) Electrolyse à travers des membranes par lesquelles s’échangent les ions en mi-lieu acide.
b) Electrolyse à basse température en milieu alcalin.
Il existe actuellement des électrolyseurs, employés dans l’industrie qui sont capables de produire 750 m3 d’hydrogène par heure : intensité 6 600 ampères, tension 540 volts.

Fig. 2. Installation d'électrolyse sons pression pour 5 100 m3 N/h d'hydrogène. (Document Lurgui).

Fig. 3. Disposition des cellules d'électrolyse sous pression. (Document Lurgui).
L’énergie nécessaire est de 4,3 à 4,7 kWh par M produit ce qui correspond à un rendement de conversion de 50 %.
Dès 1948 la firme Lurgi (1) parvint à construire des électrolyseurs industriels capables de produire l’hydrogène à la pression de 33 bars ce qui dispense bien souvent d’une compression ultérieure comme c’est nécessaire dans une électrolyse habituelle.
Quant aux Américains (General Electric Company (2), ils envisagent de construire vers 1985 des électrolyseurs par modules de 5 MW pour des projets de 100 MW et plus afin de produire de l’hydrogène grâce à des centrales nucléaires ou à des stations solaires importantes (même si ces 2 filières semblent opposables par certains, le même but est recherché.)
La C.H.E.M. System Inc, 747 Third Avenue New-York propose dès maintenant une station d’électrolyse dont la puissance est de 506 MW.
L’E.D.F. prévoit des électrolyseurs de 444 MW pour utiliser le courant électrique « heures creuses » des centrales nucléaires qu’il n’est pas possible d’arrêter quotidiennement.
c) Electrolyse de la vapeur d’eau à 850°C, avec électrolyte solide, le rendement est de 60 à 80 % et pourrait atteindre 90 % d’après la General Electric Company (U.S. A.) et l’institut Batelle à Genève (Suisse).
Nous avons obtenu 90 % en recyclant les chaleurs d’électrolyse à notre station solaire.
Dans un tel processus, une station solaire est capable de produire de la vapeur d’eau pour entraîner un turbogénérateur produisant l’électricité requise pour l’électrolyse et la température de 850°C grâce à un concentrateur.
d) Pyrocatalyse de l’eau : c’est le procédé le plus direct de décomposition de l’eau à moyenne température.
(4) — Par gazéification du charbon
Ce procédé n’est peut être pas fondé à très longue échéance suite à l’épuisement de la houille, mais il est capable de produire de l’hydrogène et du méthanol (CH3OH) dont le pouvoir calorifique est de 5 340 Kcal par kg.
(5) — Par cracking direct de l'eau (thermolyse à 2 500°C)
Un réacteur solaire est capable de produire directement l’hydrogène mais la tenue des matériaux à une telle température et la séparation hydrogène - oxygène posent des problèmes.
(6) — Par décomposition thermochimique
Plus de 2 000 cycles ont été recensés ; nous avons déjà cité celui qui utilisait l’oxyde de fer comme catalyseur.
Des recherches actives sont menées au centre de l’Euratom à Ispra (Italie)
Madame Hardy, Messieurs De Beni, et Marchetti sont parvenus à décomposer l’eau à 750°C par le cycle suivant :
Ca Br2 + 2 H20 - Ca (OH)2 + 2 HBr à 730°C Hg + 2 HBr - Hg Br2 + H2 / à 250°C Hg Br2 + Ca (OH) - Ca Br2 + HgO + H20 à 200°C HgO — Hg + 1/2 02/
(rendement 55 %)
De même à l’université d’Aix la Chapelle, au centre nucléaire de Julisch en Alle-magne, ou au Gaz de France avec le cycle du potassium :
K2 02 + H20 - 2 KOH + 1/2 02 / à 150°C 2 KOH + 2 K - 2 K20 + H2 / à 700°C 2 K20 - K202 + 2 K à 1000°C
Aux Etats-Unis : General Electric, Atomics International, Gulf General Ato- mics, Institute of Gas Technology et Division Allison de la General Motors Company avec la formule :
Cl2 + H20 - 2HC1 + 1/2 02 à 700 - 800°C 2 HC1 + 2 VC12 - 2 VC13 + H2 à 100°C
4 VCb - 2 VC12 + 2 VC1„ à 700°C
2VCi„ - 2VC13 + Cl2à 100°C
Actuellement on obtient encore mieux que ces trois formules en associant l'électrolyse à la thermochimie c’est encore là un aspect supplémentaire qui montre qu’une station solaire doit être polyvalente et un véritable complexe « électrochimique solaire ».
Monsieur A. Vialaron, directeur du programme « P.I.R.D.E.S », au CNRS de Toulouse, estime que les cycles hybrides (thermo et électrochimiques) de décomposition de l’eau présentent un intérêt et nous précise que Westinghouse (USA) et EU-RATOM (Europe) travaillent sur un cycle de décomposition de l’eau par électrolyse, associé à un cycle d’oxydo-réduction.
Dans la plupart de ces procédés réside l’intention de fabriquer l’hydrogène à partir de la chaleur d’un réacteur nucléaire sans passer par l’électricité. Un projet de GDF et du CEA concerne la production de 48 tonnes d’hydrogène à l’heure grâce à une centrale nucléaire de 3 000 MW, couplée à un cycle au potassium. Mais on se heurte sérieusement au problème de la tenue des matériaux et à la sécurité...
En revanche un réacteur solaire peut travailler à 1 000°C, sans être tributaire des nombreux échangeurs nécessaires pour assurer la sécurité si la source thermique est nucléaire, d’autant qu’il est fait usage de produits toxiques, corrosifs ou explosifs tel que le potassium.
L’un des objectifs de la station solaire d’Atlanta (USA) est aussi d’expérimenter les méthodes de décomposition de l’eau en hydrogène et en oxygène.
D’autre part, dans les réactions thermochimiques, les corps doivent y être recyclés ou utilisables dans d’autres applications.
(7) La photosynthèse artificielle.
Bien que la solution soit simple comme nous l’avons vu dans le chapitre 7, les rendements sont assez faibles dans le spectre de l’infra-rouge.
Au CEA de Saclay, MM. Guillemot et Bourrasse ont obtenu de bons résultats avec 90 % de transformation des ultraviolets en hydrogène mais les ultraviolets sont en faible proportion dans le rayonnement solaire. Il n’est pas exclu de penser que les rayonnements radioactifs de longueur d’onde plus courte que les ultraviolets peuvent produire de l’hydrogène rentablement.
A l’Institut de technologie chimique de Californie à Los Angeles, un produit chimique à base de rhodium, tranforme directement le rayonnement solaire en hydrogène, les recherches se poursuivent afin de trouver un autre métal que le rhodium car il est très coûteux, il appartient au groupe VIII (cobalt, nickel, platine).
(8) Production d'hydrogène par radiolyse avec un laser.
La décomposition de l’eau s’effectue dans un appareil très complexe à une température comprise entre 260 °C et 285 °C à une pression de 65 à 70 bars et avec un flux moyen de neutrons de 2,5 x 10'2, de rapidité supérieure à 1 MeV/cm2 sec, la puissance d’alimentation du laser est d’environ 100 MW.
Cette solution semble économique mais trop longue à décrire (pages 177 à 201, IAHE, volume 3, n° 2, 1978, IRT Corporation).
(9) Production d'H2, par cracking de l'ammoniac.
Il est possible de séparer ce gaz en hydrogène et en azote mais en général c’est l’opération inverse qui est réalisée pour la fabrication des engrais azotés (37 millions de mètres cubes d’H2 en Amérique en 1973).
(10) Séparation de gaz de fours.
Après lavage à l’azote liquide ces gaz contiennent de 80 à 90 % d’H2, cette méthode est habituelle.
Valeur de la production maximale théorique
Quel que soit le procédé d’obtention de l’hydrogène à partir de l’eau et dans l’hvpothèse où l’installation serait placée dans les conditions les plus favorables, comme par exemple dans le désert Nord du Chili où l’on relève 1 mm de pluie et 364 jours de soleil par an, nous aurions une production de 800 m3 d’hydrogène par m2 par an soit pour un carré de 10 km de côté : 80 milliards de m3 ou 30 millions de TEP par an.
Comme il est malheureusement impossible d’obtenir un rendement égal à 1, mais en toute logique 0,5, voire même 0,2, on peut diviser par 2 ou par 5 les précédentes quantités.

Fig. 4.— L'hydrure d’alliage fer-titane est un composé chimique contenant de l’hydrogène : Une façon simple de remplir le réservoir d'un véhicule. (Document Billings Energy Corporation U.S.A.)
Cette sorte d’« éponge » est contituée par du cobalt, du nickel et un composé de terres rares : Lanthane, Néodyne.
1 dm3 d’hydrure de titane stocke 1 690 litres d’H2. De nombreuses recherches sont entreprises actuellement et commencent à aboutir : chez Batelle à Genève, au Brookhaven National Laboratory (U.S. A) avec un mélange titane - fer- hydrogène, chez Philips en Hollande : lanthane - fer - hydrogène ; dans ces deux cas la capacité est de 180 cm3 d’hydrogène à la pression de 2 bars, par gramme d’alliage.
Au Japon : MATSUSHITA Industrial Research Institute à récemment mis au point un alliage à base de titane, zirconium, chrome et manganèse obtenu au four électrique à arc, sous argon ; la capacité de stockage est de 200 cm3 d’H2 à 30 bars par gramme d’alliage dont le prix est de 3 yens/gramme.
II y a plus de 20 brevets sur cette question.
Le stockage d’hydrures ne pose pas davantage de problème que celui du fuel ou de l’essence dans le réservoir d’un véhicule.
La disposition est totalement différente afin que la chaleur du moteur puisse chauffer l’hydrure.
Le prix d’investissement de l’hydrure varie entre 20 F et 130 F le kilogramme, pour un rapport poids / masse H2 variant de 3,5 (le Mg2 Ni Hj4) à 12,7 (le LiH).
L’hydrure est une sorte de second réservoir dont le prix importe peu puisque c’est comme une consigne.
En 1979, 100 kg de LiH équivallent à 61 litres d’essence. (Une très importante étude sur le sujet : pages 411 à 442 par J. Donnely, W.C. Greayer, J. Nichols, de PAérospace Corporation California, de W. J.D. Escher et E. Ecklund respective¬ment de la Escher Technology A. St Johns, Michigan, et de l’U.S. Département of Energy, Washington. Volume4 n° 5 - 1979 de l’IAHE.
Réf : Institut Français du Pétrole (I.F.P.)
1 et 4 Av. du Bois Préau 95502 Rueil-Malmaison.

Fig. 4 bis. — Pile à combustible « Pratt et Whitney » type PC1I. Puissance 12,5 k W, couplée à titre d'expérience au réseau d'Hydro-Québec.
LES UTILISATIONS DE L’HYDROGENE
1) Chauffage des locaux : Grâce à une chaudière à gaz qui complétera ce que l’énergie solaire n’aura pas pu fournir sur le lieu même de l’utilisation (chauffage complémentaire de maisons solaires).
Le réseau de gaz de ville à Paris contient 50 % d’H2.
Beaucoup d’industriels qui ont modifié leurs brûleurs de chaudières afin d’utiliser le gaz naturel, pourront très facilement s’adapter à l’H2 ce qui augmentera la longévité du matériel.
2) Electricité
Grâce à une pile à combustible (il ne faut pas oublier que l’hydrogène est un métal qui va se « ronger » de la même façon que le zinc d’une pile sèche, mais avec cette différence qu’il est facile de le renouveler en introduisant plus de gaz), on peut produire de l’électricité avec un rendement de 40 à 80 %.
D’après Pratt et Whitney à Hartford (USA) qui est l’un des mieux placés des constructeurs mondiaux, et en accord avec le programme américain « Target » financé par une trentaine de compagnies de gaz. (Photo fig. 4 bis).
C’est en 1802 que Davy, et Grove en 1839, trouvèrent la réversibilité de l’électrolyse de l’eau ; aujourd’hui la puissance massique des piles à combustibles est de 500 watts par kg contre 5,4 W/kg en 1965.
Avec les piles à hydrazine que fabrique Alsthom, la puissance massique dépasse 1 000 watts par kg.
Or la puissance massique d’un moteur d’automobile est en moyenne de 350 watts par kg, ce qui autorise la comparaison en tenant compte du poids du moteur électrique et de celui du réservoir d’hydrures.
Partout où nous aurons besoin d’électricité, la pile à combustible dont la puissance peut atteindre plusieurs mégawatts, peut rendre de grands services : centrale de secours dans les entreprises qui utilisent des ordinateurs, groupe électrogène sans chaleur ni bruit, ce qui est d’un intérêt évident pour les militaires.
La pile à combustible paraît difficile à généraliser en raison de l’utilisation d’un métal rare, le platine. On ne peut guère envisager que le procédé du professeur Justi, lequel emploie le nickel, mais il faut des gaz sous pression. Le générateur n’est plus du ressort des installations individuelles.
Malgré un marché assez restreint jusqu’à présent, le prix des piles à combustibles varie de 250 à 1000 F le kilowatt installé ce qui est compétitif avec les petits groupes électrogènes à moteur à explosion.
3) Métallurgie
De même que le charbon est un réducteur des oxydes métalliques, l’hydrogène l’est aussi, il est déjà employé à Mexico chez ARMCO, et en projet au Japon.
4) Chimie :
Pour la synthèse de l’ammoniac dont l’utilité est de fabriquer des engrais, pour la fabrication du méthanol (en association avec le carbone et l’oxygène, puisque sa formule est CH3 OH), et qui est un excellent carburant pour un véhicule actuel.
Deux litres de méthanol cela équivaut à un litre d’essence.
5) Alimentation.
L’hydrogène peut servir sous forme de protéines dans les levures « hydrogé-nomonas » afin de nourrir les animaux.
L’H2 est utilisé pour l’hydrogénation des huiles, la fabrication de la margarine.
La demande a été de 10 millions de m3 en 1973 et sera de 20 millions en 1980, pour ce secteur, aux USA.
6) Industrie du verre, de l’acier, de l'électronique, du pétrole et autres.
La température de combustion de l’H2 et sa vitesse de propagation (inférieure à celle de l’acétylène), sont mises à profit pour travailler certains verres techniques, comme la fabrication continue des glaces sous atmosphère d’azote H2 (chez Bous- sois).
Avec l’H2 on peut découper l’acier sous l’eau, la fonte, l’acier inox.
Procéder au soudage des alliages au chrome, manganèse, titane, sans oublier le soudage dit à « l’hydrogène atomique » (qui n’a rien de radioactif).
En électronique signalons le traitement des diodes à jonction sous atmosphère azote-hydrogène.
Pour éliminer le soufre des produits pétroliers les raffineries utilisent l’H2 (115 millions de m3 en 1980 aux USA).
Dans la fabrication du caoutchouc, le refroidissement des gros alternateurs, le gonflage des ballons d’observation (le CNRS, CEA, CNET, CNES envisagent le retour des dirigeables gonflés à l’hélium pour transporter des charges jusqu’à 500 tonnes.
L’ingénieur Nazare est l’auteur d’un brevet à ce sujet), dans les chambres à bulles ex : « Mirabelle » la plus importante du monde, livrée par le CEA à l’URSS, on utilise sans problème l’hydrogène.
7) Carburant pour véhicule.
— Sous forme d’hydrure ou de poudre : 100 kg d’hydrures équivalent à 61 litres d’essence. Pour un véhicule de poids total : 1 080 kg, l’autonomie est de 350 km.
— Sous forme comprimée dans des réservoirs en acier : autonomie 200 km, à la manière des véhicules qui fonctionnent au gaz dans le sud-ouest en particulier
(fig. 5 et 6).
La ville de St Etienne a décidé en juillet 1979, d’équiper progressivement au gaz ses 170 véhicules de service qui consomment 160 000 litres de super par an.
La ville de Nantes prend la même décision en octobre, beaucoup d’autres suivent rapidement cette idée.
Le moteur à gaz n’est pas seulement réservé à la locomotion puisque la ville de Rennes utilise depuis 1977 les gaz d’égouts pour alimenter les moteurs qui produisent l’électricité nécessaire à l’usine d’épuration.
L’économie ainsi réalisée est de 450 tonnes de fuel par an.
La généralisation du procédé devrait en 1985 économiser 20 000 tep par an en France.
Toutes ces adaptations au gaz montrent combien elles préparent l’ère de l’hydrogène.
— Sous forme liquide pour effectuer des trajets réguliers, comme les transports urbains, SNCF etc. car autrement il y aurait évaporation de l’H2 suite au réchauffement pendant le stationnement prolongé.

Fig. 5.— L'équipement d'un véhicule au gaz naturel est déjà pratiqué en France (50 000 U.) et dans beaucoup de pays d'Europe : Hollande, Italie (260 000 11).
(Document Sic» l’Air l iquide).

Fig. 6.— Station de distribution de gaz naturel liquéfie Aux Quatre Pavillons (Sortie nord de Bordeaux).
(Photo J.-L. Perrier).
7.1) . Les véhicules Mercedes-Daimler-Benz (fig. 7, 8, 9).
De très importantes études ont abouti à la réalisation de plusieurs véhicules alimentés avec de l’essence et de l’hydrogène à partir de réservoirs hybrides contenant de l’hydrure comme par exemple figure 10.
Avec 200 kg d’hydrure de Mg H2 stockant 16 kg d’H2 soit l’équivalent de 77 l d’essence, et 20 l d’essence, il a été possible de parcourir 600 km avec un véhicule de
2 400 kg.
Cela est satisfaisant en comparaison de la consommation d’engins similaires, comme celle du fourgon J7 (jusqu’à 17 l aux 100 km).

Fig. 7.— Mini bus à hydrogène à partir d'hydrures.
(Document aimablement communiqué par les Dr Buchner et Saüfferer)
Qu’il nous soit permis de remercier ici le Dr Buchner et le Dr Sàufferer, Directeur du programme hydrogène chez Mercedes, membres de l’IAHE, pour les très nombreux documents gracieusement remis. (Un article de 22 pages sous le titre : The Hydrogen hydride Energy Concept, est paru dans le volume 3 n° 4 -- 1978 IAHE).
De ces documents (53 pages, 21 photos) nous sommes heureux d’extraire aussi la figure 11 qui montre comment la maison « tout hydrogène — carburant auto » peut parfaitement exister.
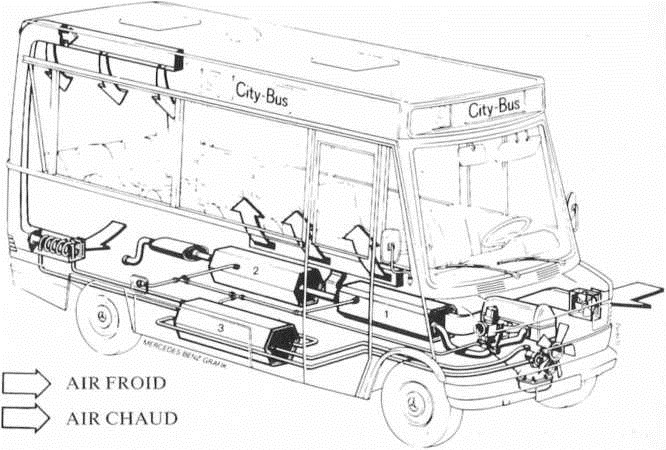
1. Réservoir de stockage d’hydrure à haute température, chauffé par les gaz d’échappement (chauffage auxiliaire)
2. Réservoir d’hydrure à basse température, chauffé par les gaz d’échappement (condensation)
3. Réservoir d’hydrure à basse température à échangeur thermique à liquide (conditionnement d’air).
Fig. 8.— Disposition des 3 réservoirs d'hydrures a des températures différentes.
La chaleur du moteur chauffe l’hydrure qui libère l'H2.
(Document aimablement communiqué par les Dr Buchner et Saüfferer)

Fig. 9.— Véhicule à hydrogène alimenté par un réservoir hybride d'hydrure-essence.
(Document aimablement communiqué par les Dr. Buchner et Saüfferer. Mercedes)
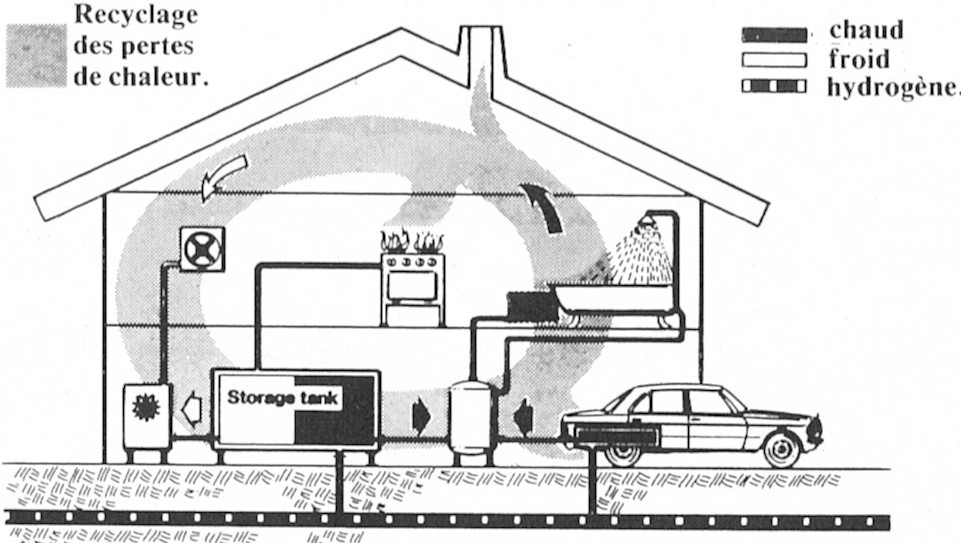
Fig. 11.— Stockage d'hydrogène dans un hydrure pour l'énergie domestique et pour celle du véhicule.
Document aimablement communiqué par les Dr Buchner et Saüfferer, Mercedes.)

Fig. 10.— Réservoir d'hydrure de la voiture décrite fig. 9.
(Document aimablement communiqué par les Dr. Buchner et Saüfferer, Mercedes).
7.2) . Le véhicule Billing.s Corporation (fig. 12).
Plusieurs mini-bus de 21 passagers sont en service expérimental dans la ville de Provo.
Le moteur Dodge d’une cylindrée de 7 200 cm3 est alimenté avec de l’H2 venant d’un réservoir d’hydrure de Ti Fe et une injection d’eau.
Une étude de rentabilité sur 100 mini-bus parcourant 480 km par jour indique que dès la 1ere année on économise 5 000 dollars ; pour une période de 5 ans le transport à l’H2 coûte 2,27 fois moins qu’avec l’essence (et en tenant compte des travaux d’adaptation).
Fig. 12.— Véhicule américain à l'hydrogène et à l'eau (cylindrée 7 200 cm3). (Document Billings Energy Corporation U.S. A.).

L’étude de Billings montre que l’écart entre l’augmentation du prix de l’essence et la diminution de celui de l’H2 (0,9 en 74) sera de 1,69 en 1985 ce qui prouve que la rentabilité annoncée sera supérieure à 2,27 dans les 20 ans futurs.
Ensuite il ne sera même plus question de comparer les prix, il y aura pénurie d’essence mais pas pour l’H2 (l).
Comparaison des rendements mécaniques dans un moteur :
Hydrogène 33 %
Méthanol 28 %
Essence 25 %
Electricité 80 % (pour un véhicule)
(1) En janvier 1980, Billings commercialise des Chrysler Omni (l’équivalent US de la Tal- bot Horizon) munies d’un dispositif d’alimentation essence ou hydrogène par simple commutation sur un bouton du tableau de bord.
Le générateur d’hydrogène est vendu avec la voiture et il se branche sur le 220 V, comme un véhicule électrique mais les performances de légèreté, de fiabilité, d’autonomie (170 km) et de vitesse (130 km/h) confèrent au véhicule à l’H2 une avance technologique.
Billings Energy Corp. va bientôt proposer sur le marché des kits d’adaptation.
Mais pour l’instant le rendement de stockage n’est guère favorable à l’électricité.
Hydrogène 95 % Méthanol 95 % Electricité 49 % (accus).
Hydrure 90 % Essence 95 %
7.3). Véhicule J.L. Perrier(l) (fig. 13, 14)


Fig. 13.— Le véhicule à hydrogène par J.-L. Perrier devant le concentrateur solaire produisant de l’hydrogène.
(Photo J.-L. Perrier et J.-M. Boullet).
(1) Présenté à la presse le 19 janvier 1979. réf. : La Nouvelle République, Ouest France, du 20, 21 janvier, Le Courrier de l’Ouest du 20, 21 et 23 janvier, L’Aurore du 28 janvier, Solaire Magazine du 3 avril, Presse Océan du 10 mai, Science et Vie de juin 79, L ’Express du 4 août, Sud-Ouest : (feuilleton d’une semaine fin décembre 79) etc...
Emissions de télévision 3,5 mn : 16 mars FR3, et 20 juin A2. Une communication sur ce véhicule a été faite au congrès international à l’université de Miami (Floride USA) 16, 17 avril 1979 au siège de l’IAHE, ce qui a donné lieu à un article dans la Revue internationale pour l’hydrogène, pages 444, 445, volume 4 n° 4, 1979.
Présenté au musée de Poitiers avec démonstration place de l’Hôtel de Ville, le 23 janvier 1980 grâce à l’obligeance de Monsieur le Conservateur du Musée, de Monsieur De Litardière, des Professeurs Bauer et Brochet, de nombreuses autres personnalités et de l’aide de Monsieur le Directeur Départemental de la Jeunesse des Sports et des Loisirs de la Vienne.
Présenté à la Foire de Paris du 26 avril au 3 mai 1980 grâce à l’aide efficace de M. Fougeron, Comité d’Action pour le Soleil, 7, rue du Laos, 75015 Paris, et dans l'Auto-journal, n° 1117 du 17 mai 1980.


Fig. 14.— l es circuits d'alimentation d'hydrogène sont signalés par des cercles. Moteur H2
J.-L. Perrier.
(Photo J.-L.. Perrier et J.-M. Boullet).
L’intention de l’auteur était de prouver que l’énergie solaire n’était pas seulement un mode de chauffage mais un moyen de transformer l’eau en hydrogène et de l’utiliser directement comme carburant, ou de fabriquer du méthane, du méthanol qui sont aussi des carburants.
Ce véhicule est l’un des premiers à fonctionner à l’hydrogène pur, en France en 1979.
L’adaptation comporte différents circuits à des pressions différentes pour amener l’H2 dans le venturi du carburateur par 3 tubes.
Lors des essais et afin de dissiper la mauvaise réputation du moteur à eau dont Perrier, en dépit de son nom, n’a jamais été l’auteur, a utilisé de l’hydrogène gazeux, acheté à la Société l’Air Liquide qui lui a accordé un contrat. De cette manière on ne pouvait mettre en doute la nature des gaz employé par J.L.P., membre de l’Association Internationale pour l’Energie à l’Hydrogène (IAHE).
Six mois plus tard, J.L. Perrier fabrique lui-même l'H2 à sa station héliotechnique en utilisant un cycle thermodynamique, réalisant ainsi une première mondiale qui est décrite à la 4e partie de cet ouvrage.

7.4) . Véhicule à hydrogène liquide (fig. 15)
La Datsun B 210 équipée en 4 mois à l’H2 liquide possède un réservoir de 230 litres à la pression de 5 bars qui est capable de résister à des décélérations de 10 g en cas de collision.
Ce véhicule possède une autonomie de 650 km, sa vitesse est comprise entre 80 et 88 km/h. L’essai d’endurance sur 2 781 km a montré le parfait fonctionnement du moteur qui avait été modifié (arbre à cames supplémentaire d’injection d’H2).
La conclusion des chercheurs japonais Furuhama, Hiruma et Enomoto, à l’issue d’un rapport de 21 pages (volume 3-1 1978 IAFIE) c’est que le transport de l’H2 ne pose aucun problème notable de sécurité ni de fonctionnement et que la pollution est très très faible.

Fig. 16.— Véhicule à hydrogène liquide (présenté le 9-3-1979).
(Document aimablement communiqué par le Dr. Y. Enomoto, Tokyo)
Les chercheurs de la Misashi I.T. pensent que l’alimentation des véhicules par cassettes d’hydrogène liquide est une bonne solution pour l’avenir.
Le 9 mars le Musashi I.T. présente à la presse une auto 550 Suzuki (fig. 16) dont la vitesse peut atteindre 120 km/h, toujours à l’H2.
C’est ce que nous avons appris par un article du Herald Tribune du 10.3.79 aimablement communiqué par le journaliste américain Mark Antman.
Dans sa déclaration à la presse, M. Enomoto exprime son regret de ne pouvoir tester ce véhicule sur les routes du Japon. (Notons que l’essai avec la Datsun B 210 avait été réalisé aux USA entre Bellingham, Los Angelès, Santa-Cruz et Santa Bar-bara).
Outre les nombreuses photos adressées par notre collègue de l’IAHE avec l’autorisation de diffusion, ce dont nous le remercions, le Dr Y. Enomoto a bien voulu nous faire part de la communication de 7 pages proposée au XVe congrès international du froid à Venise (23-29 septembre 1979) sous le titre « véhicule à hydrogène liquide à moteur deux temps à injection et allumage par bougie.
Cette solution présente beaucoup d’avantages, notamment :
— Faible travail de compression grâce à l’utilisation de la pompe à hydrogène liquide.
— les parties surchauffées du moteur peuvent être refroidies par l’H2 à basse température.
— L’énergie de pression de l’H2 injecté et de sa vaporisation (42 % en plus du volume du mélange initial) peut être transformée en puissance utile.
Bien que la longévité des injecteurs et de la pompe à H2 liquide reste à prouver, les chercheurs japonais s’attendent à ce que le moteur à injection à deux temps soit le meilleur pour les voitures à hydrogène.
7.5) . Le moteur diesel à hydrogène
Les chercheurs H.S. Homan de l’Université de Princeton, W. J. Me Lean de l’Université Cornell à Ithaca et R.K. Reynolds de la Jet Propulsion à Pasadena aux USA ont expérimenté un moteur diesel D 399 de la célèbre marque Caterpillar en adaptant des injecteurs à l’hydrogène gazeux. Le taux de compression : 29, suffit à provoquer l’auto-allumage (927°C).
Le moteur diesel est largement employé dans les engins industriels, l’adaptation à l’H2 revêt donc ici une importance encore plus grande.
(Références : 11 pages en anglais volume 4 n° 4 — 1979 IAHE dont ces chercheurs sont également membres).
Les exploitations agricoles peuvent utiliser le méthane produit par le fumier et les déchets végétaux par fermentation mais aussi l’hydrogène.
7.7) . Observations diverses sur les moteurs H2.
La conversion d’un moteur ordinaire à l’hydrogène est assez délicate, réalisable la preuve en est, mais au prix d’efforts assez importants comme dans tout prototype.
La description détaillée de tous les dispositifs nécessiterait plusieurs milliers de pages (le lecteur pourra se procurer les nombreux livres auprès de l’IAHE qui sont diffusés par Pergamon Press (Oxford, New York, Frankfort). Certains coûtent jusqu’à 600 dollars soit environ 3 000 F.
En résumé, le moteur à H2 est 30 % plus puissant que celui initialement à l’essence, sa vitesse de ralenti est très basse si on le désire à cause de l’excellent mélange gaz-air. Au démarrage il n’y a pas de « lavage » des cylindres comme c’est le cas avec le starter, responsable d’un excès d’essence.
Le graissage sera donc meilleur mais il faudra choisir une huile plus fluide, 10 SAE de moins, car elle a tendance à épaissir sous l’action de l’H2.
Le moteur aura une longévité plus grande, comme dans le cas des moteurs à gaz naturel liquéfié GNL ou GPL avec le butane- propane.

Fig. 17.— M. Georges Romney, ancien P.D.G. du bureau de VAmérican Motors et Gouverneur du Michigan, et M. Roger llillings sur un tracteur Jacobsen alimenté à l'hydrogène.
(Document I.A.H.E.)
Le moteur à H2 n’est pas polluant, il ne rejette pas d’oxyde de carbone, ni de gaz carbonique et seulement 40 fois moins d’oxyde d’azote (gaz hilarant).
Le principal rejet dans l’échappement c’est la vapeur d’eau ; l’eau initialement utilisée lors de sa décomposition dans l’électrolyseur par exemple.
Que le lecteur se rassure, on ne risque pas les inondations sur les routes, ce qui sort du tuyau d’échappement présente la même apparence qu’avec l’essence.
Il est vraiment navrant d’entendre ou de lire que le moteur à hydrogène mouillera les routes, qu’il faudra des essuie- glaces renforcés, pourquoi pas aussi des hélices aux véhicules, comme sur les bateaux ?
Le calcul indique qu’une auto de 8 à 9 ch fiscaux rejette 0,2 litre d’eau au km soit environ 1 goutte d’eau par mètre parcouru, sous forme de vapeur. Le moteur essence, les réacteurs d’avions (trainées blanches) rejettent aussi de la vapeur d’eau.
Le constructeur automobile Ford a signé avec Philips en 1972, un contrat exclusif mondial, pour un moteur Stirling à hydrogène.
La Régie Renault poursuit des essais sur un moteur 1 300 cm3 à l’H2.
En 1945 un camion Saurer 1918 a fonctionné à l’H2 dans la région de Saumur grâce aux talents de MM. Hubault et Dubled.
Christian Reithmann construisit à Monaco en 1858 un moteur à H2 qu’il transforma ensuite au gaz d’éclairage.
L’adaptation du moteur à piston revêt une grande importance afin de ne pas réformer les chaînes de fabrication ni les véhicules existants.
Mais dans un avenir relativement proche il est possible que la pile à combustible (rendement global 50 %) puisse alimenter des moteurs électriques placés dans les moyeux des roues.
Pendant le freinage, les moteurs deviennent des générateurs de courant électrique, la pile travaille alors en électrolyseur d’où remplissage du réservoir.
A partir de 1985, des piles à hautes performances, et surtout vers 1990 les accus lithium/aluminium/sulfure de fer (175 W/kg au lieu de 30 avec les accus actuels pour le même prix et d’un rendement de 90 %) feront une grande révolution dans le domaine de l’automobile : véhicule plus léger, silencieux, non polluant, d’un rendement global de transmission : 64 %.
Pour un même nombre de véhicules en circulation on dépensera presque 3 fois moins de carburant.
La conclusion des 32 pages du rapport très intéressant (vol. 4 n° 5 — 1979) de M. J. Donnelly et de ses collègues, déjà cités à propos des hydrures, c’est que dans la période 85 à l’an 2000, une automobile 4 places, roulant à l'H2 sera plus légère, moins coûteuse, la sécurité devra être envisagée surtout lors du stationnement d’où une bonne aération des garages et des parkings souterrains ; la plus grosse difficulté concerne l’implantation rapide d’un réseau de distribution d’hydrures et de points de ravitaillement d’H2, on trouve exactement le même problème actuellement avec le GNL ou le GPL.
A court terme, la voiture électrique est trop lourde, encombrante, de faible autonomie et coûteuse, par contre après l’an 2000 la différence sera moins importante.
Il apparaît qu’il faut produire de l’H2, c’est dire l’importance de l’énergie solaire dans sa production en grandes quantités.
Cette notion est développée par exemple dans la revue du service d’information de Monsieur le Premier Ministre (juin 1979) lequel signale en bibliographie la lre édition du livre de J.L. Perrier ; qu’il en soit respectueusement remercié.
Alors que les Américains prévoient une production de 2 189 millions de m3 d’H2 en 2000, la Commission des Communautés Européennes avait proposé un budget de 13 millions d’EUA soit environ 16 millions de dollars pour un programme de recherche sur l’hydrogène pour la période 1975-1980 (Réf. G. Imarisio, p. 371 à 375 vol. 4/5 1979 IAHE) .
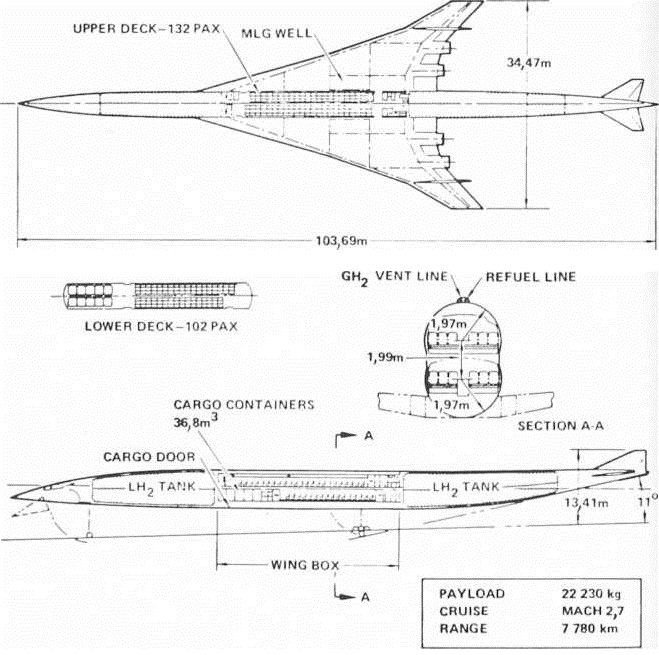
Fig. 20.— Projet d'avion à hydrogène liquide volant à mach 2,7 capable de transporter 234 passagers sur 7 780 km
(Document aimablement communiqué par le Dr. G.D. Brewer. Lockheed U.S.A.)
On remarque dans la figure 19 que les réservoirs d’H2 sont éloignés des réacteurs, d’où moins de risque qu’avec le jet A qui se trouve normalement dans les ailes, tout près de la flamme des tuyères.
Un autre projet concerne un avion supersonique volant à mach 2,7 (figure 20), il serait capable de transporter 234 passagers sur 7 780 km. Le poids de cet avion au décollage, 179 tonnes, au lieu de 345 t avec le jet A.
Cette différence de poids importante (166 t) provient de ce qu’il faudrait 150 t de jet A (alors qu’avec l’H2 il faut 38,7 t), mais aussi de ce que la structure de l’avion est plus légère suite à une différence de 111 t de carburant.
Doc. NASA aimablement communiqué ». par- le Dr R F KORYCINSKY de la NASA N
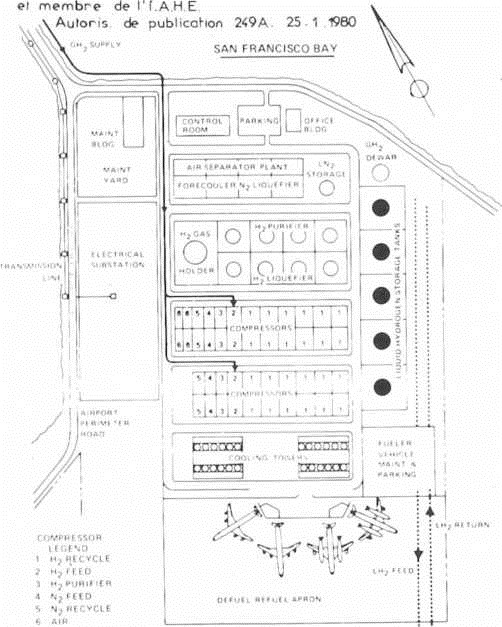
Fig. 21.— Equipement de l'aéroport de San Francisco (U.S.A.) pour distribuer 1 000 t d'hydrogène liquide, soit l'équivalent de 3 0001 de jet A actuel.
(Document P.F. Korycinski, Nasa).
La surface portante des ailes passe de 1031 m! à 739 m2 (plus un avion est lourd, plus il faut des ailes, un train d’atterrissage importants, etc...) Le poids engendre le poids et néces¬site davantage de carburant.
Par contre L’hydrogène est multiplicateur de la légèreté :
1 m3 d’H2 pèse 70,8 kg, 1 m3 de jet A = 877 kg.
Si le volume occupé par l’H2 est 4 fois plus important qu’avec le jet A, ce n’est pas très gênant, on allonge un peu le fuselage (1/10 de sa longueur) ce qui permet d’y loger l’H2 en l’éloignant
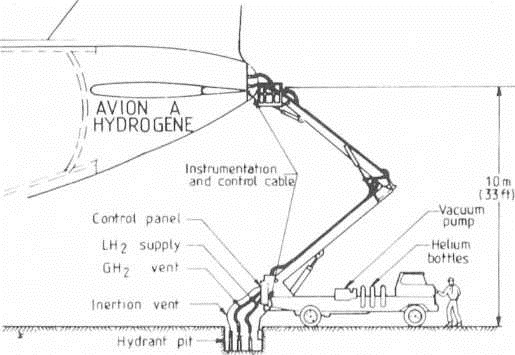
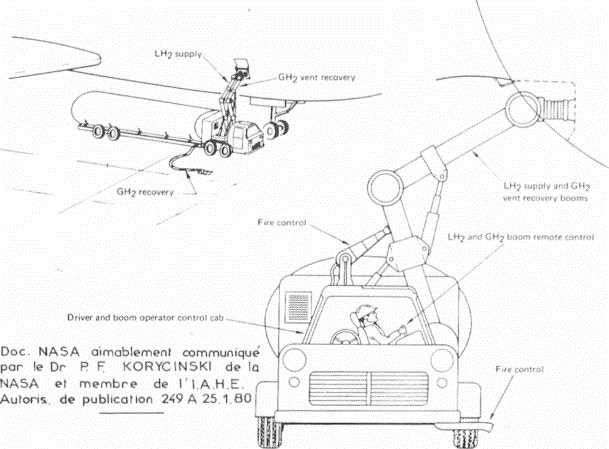
Fig. 22.— Les raccords normalisés existent pour le remplissage d'hydrogène liquide ainsi que
les véhicules spéciaux.
(Document P.F. Koryanski, Nasa)
Des réacteurs, d’où une meilleure sécurité en comparaison du jet A qui est dans les ailes. Ce qui compte surtout dans un avion ce n’est pas tellement le volume, mais surtout le poids. Comme la masse de l’avion est moins grande, et que la poussée des réacteurs est supérieure, la distance de décollage est réduite de 3 000 m à 1 500 m.
Quant au prix d’un avion à l’LH2, il est le même pour un appareil volant à mach 0,85 (fig. 14) mais devient 1,35 fois moins pour le projet volant à mach 2,7 (45,5 millions de dollars contre 61,5 avec le jet A).
Les experts de la Lockheed et de la Nasa estiment que l’avion à l’LH2 offre la même sécurité que les autres, il sera plus maniable suite à sa légèreté, il polluera très peu et économisera l’énergie.
L’équipement des aéroports ne relève pas de la fiction comme nous pouvons le voir : (fig. 21-22), d’après un rapport de 20 pages de l’ingénieur P.F. Korycinski, Nasa, dans la revue de PIAHE Vol. 3 — n° 2 — 1978.
Toutes les recherches faites par la Nasa pour la conquête de l’Espace, grâce à l’LH2, sont directement et rapidement exploitables pour l’aviation militaire et civile. Les raccords standards et les modes de remplissages existent.
Quant à l’énergie électrique nécessaire à l’électrolyse, elle est de 332 MW à San Francisco et de 350 MW à l’aéroport de Chicago.
L’LH2 sera produit aussi par gazéification du charbon au début.
AVANTAGES DE L’HYDROGENE D’ORIGINE SOLAIRE :
Jusqu’à présent l’hydrogène provenait d’une énergie ou d’un combustible coûteux qu’il était préférable de consacrer à autre chose (fuel, électricité)...
L’épuisement des sources énergétiques et même des matières premières incite à se tourner vers l’hydrogène qui est de plus un combustible non polluant lors de sa production en prenant les précautions d’usage.
Quant à l’utilisation, au moment de la combustion il y a une légère quantité d’oxyde d’azote (moins dangereux que.l’oxyde de carbone vu les proportions), pratiquement pas si l’on utilise la pile à combustible, et toujours restitution de l’eau initialement investie sans déséquilibre de la quantité d’oxygène que comporte la nature.
Même si l’oxygène produit au moment de la décomposition de l’eau, est employé en chimie, l’appauvrissement sera beaucoup plus faible qu’avec la combustion massive de produits pétroliers. L’industrie nucléaire a peut être des inconvénients mais on ne peut pas lui reprocher de consommer l’oxygène de l’air.
L’hydrogène constitue un vecteur énergétique inépuisable car très rapidement recyclable :
1 m3 d’eau contient 888 l d’oxygène, 111 d’hydrogène et 1 de divers corps, c’est- à-dire l’équivalent énergétique de 470 litres d’essence à condition toutefois de dépenser une énergie encore plus grande au moment de l’électrolyse ou du cracking thermochimique pour séparer l’hydrogène de l’oxygène. (Pour soulever une pierre il faut dépenser de l’énergie mécanique, si on la laisse tomber, cette énergie sera res-tituée).
1 km3 d’eau contient en hydrogène l’équivalent de 470 millions de m3 d’essence (il serait plus logique de dire que ce kilomètre cube d’eau résulte de la combustion des 111 millions de tonnes d’hydrogène (= 470 d’essence) et qu’il s’agit d’un état énergétique dégradé et non potentiel, exactement comme lorsque la pierre est en bas.
La consommation mondiale de pétrole en 1980 (3 milliards de tonnes) correspond au débit moyen de la Seine (520 m3/s), pendant 83 jours... on dira que le pétrole coulait à flots en l’an 1980.
La production d’hydrogène en remplacement total du pétrole nécessiterait d’utiliser le débit du Rhône (1720 m3/s) pendant 33 jours pour fournir le monde entier et 1,3 j. pour la France.
En définitive, le vecteur énergétique de l’avenir à longue échéance s’élaborera à partir de l’eau et du rayonnement solaire, beaucoup d’applications sont possibles.
Les formes peuvent être les plus diverses : eau chaude, vapeur, méthane, méthanol, huile chaude avec un réseau de distribution urbain, électricité...
Comme le souligne très justement l’ingénieur .LA. Grégoire dans son livre « vivre sans pétrole » Ed. Flammarion, le public a tendance à faire à propos de l’hydrogène un complexe d’Hindenburg consécutif à l’incendie qui détruisit le dirigeable de ce nom, à New York, peu avant la dernière guerre mondiale. Pourquoi ne pas parler aussi du complexe de la rue Raynouard après la terrible explosion de gaz en 1978 à Paris.
Depuis cette époque la technologie a évolué, on sait utiliser parfaitement ce gaz dans l’industrie comme nous l’avons vu précédemment, dans de bonnes conditions de sécurité.
Qu’il s’agisse d’acétylène : C2 H2 — EDF-GDF veulent en fabriquer à partir du carbure de calcium et d’eau dont le pouvoir calorifique à l’état gazeux est 4 fois plus grand que PH2, du butane, du propane, du méthane, de l’essence, du méthanol, de l’alcool, tous ces produits sont explosifs, c’est bien pour cela qu’on les utilise.
Un carburant sans énergie n’est pas dangereux mais ne présente guère d’intérêt, pourquoi ne pas faire le plein de sa voiture avec du sable ?...
C’est économique et pas dangereux...
Il y aura certainement des incendies et des explosions à cause de l’hydrogène, mais pas plus qu’avec les carburants liquides ou gazeux actuels (véhicules en feu, pétroliers, avions, conduites de gaz qui explosent etc...)
A plusieurs reprises nous avons examiné la sécurité de l’H2, notamment en évoquant que sa température d’auto-allumage est plus importante (585°C) que celle de l’essence (228 à 47I°C) mais nous pouvons ajouter que :
— l’hydrogène brûle dans l’air en dégageant une température (2045°C) inférieure à celle de l’essence (2197°C).
— La diffusion des fuites d’H2, dans l’air, est plus rapide (2 cm/seconde) qu’avec l’essence (0,17 cm/s.) d’où moins de risque de stagnation du produit, d’où moins d’explosions possibles.
— La limite d’explosion est plus étendue avec l’H2 (4 à 75 %) qu’avec l’essence (1 à 7,6 %) ce qui n’est pas forcément un avantage en faveur de l’essence car l’explosion sera plus vite réalisée avec.
En effet il semble plus juste de parler de la limite inférieure à cause de la diffusion qui fait croître la concentration, plutôt que le phénomène inverse, plus rare.
— Si l’énergie minimale pour enflammer l’H2 dans l’air (étincelle par exemple) est de 0,02 mJ contre 0,24 pour l’essence, d’où effectivement un risque plus important, la majorité des sources de chaleur donne une énergie supérieure à ces deux valeurs, ce qui finalement crée le même risque, sauf peut-être avec l’électricité statique, d’ailleurs facile à éliminer. S’il y a une fuite en présence d’étincelle cela explo¬sera de toute façon mais en ne faisant pas forcément les mêmes dégâts comme nous allons le voir plus loin.
— Dans le cas d’une combustion, l’H2 rayonne 17 à 25 % de son énergie au lieu de 30 à 42 % pour l’essence et 23 à 33 % pour le méthane, d’où une propagation d’incendie moins importante pour l’H2, dont la flamme est légèrement moins chaude de surcroit.
— Si il y a explosion, les dégâts produits par l’H2 seront moins importants :
a) A l’état liquide : 1 cm3 d’LH2 équivaut à 1,71 gr de T.N.T. (L’explosif bien connu) alors que 1 cm3 de méthane (gaz naturel) équivaut à 4,56 gr de T.N.T. et 1 cm3 d’essence à 7,04 gr de T.N.T.
b) A l’état gazeux : 1 m3 d’H2 équivaut à 2,02 kg de T.N.T., 1 m3 de méthane à 7,03 kg de T.N.T. et 1 m3 de vapeur d’essence à 44,22 kg T.N.T. d’où présence de plomb dans l’essence pour éviter une explosion trop brutale.
De ce dernier tableau il apparait que l’explosion du méthane fait 3,48 fois plus de dégât que l’H2 et que les vapeurs d’essence en font 22 fois plus.
En utilisant une technologie sérieuse, l’H2 est le carburant de l’avenir, directement ou pour fabriquer des combustibles synthétiques, il est inépuisable et n’est pas cancérigène comme les produits pétroliers.
UNE REMARQUABLE PROPHETIE ?
Le romancier scientifique nantais Jule Verne avait préssenti avec beaucoup d’exactitude les voyages sous l’eau, dans l’air et même vers la Lune.
Dans son roman : « L’île mystérieuse » écrit en 1870, nous pouvons lire en résumé :
« L’eau est décomposable en ses éléments primitifs par l’électricité... Je pense que l’eau sera un jour employée comme carburant, que l’oxygène et l’hydrogène qui la constituent employés ensemble ou séparément, pourront fournir une source inépuisable de chaleur et de lumière et d’une intensité dont le charbon n’est pas capable...
Je pense que lorsque les mines de charbon seront épuisés, nous aurons à nous servir de l’eau, l’eau sera le combustible du futur... ».
Aujourd’hui, le principal combustible pour explorer l’espace est le mélange oxygène/hydrogène, raison pour laquelle la NASA en produit autant.
Une association internationale : « International Association for Hydrogen Energy (1) (I.A.H.E.) groupe des chercheurs de 26 pays, organise des congrès, séances de travail, etc... et publie une revue, sous le titre : « International journal of hydrogen Energy » dont nous extrayons dans sa version originale un schéma très explicite (fig. 23).

Fig. 23. —Abondante énergie propre pour l’humanité (Document IAHE) USA.
(1) P.O. Box 248266, Coral Gables, Florida 33124 USA. 296
(I) Référence : Hydrogène d’origine solaire par J.L. Perrier, communication faite à la XVe